[ad_1]
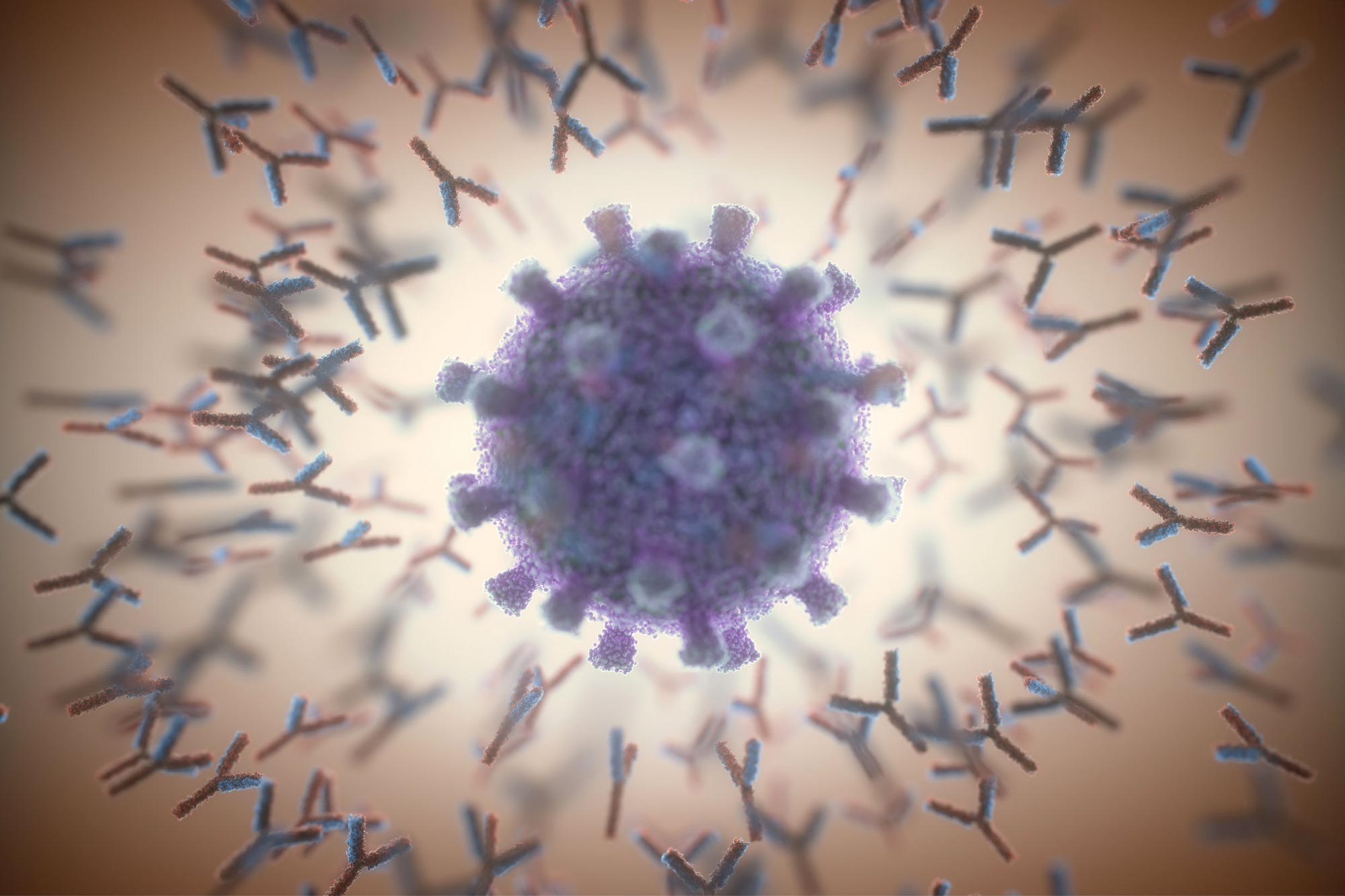
An artistic rendering of antibodies surrounding a SARS-CoV-2 particle.
Antibody therapy that seems to neutralize all SARS-CoV-2 strains, and other coronaviruses, was developed with a little help from structural biologist Jay Nix.
Save lives COVID-19[feminine les vaccins nous permettent de nous sentir à nouveau optimistes, après plus d’un an d’anxiété et de tragédie. Mais les vaccins ne sont qu’un côté de la médaille – nous avons également besoin de traitements qui peuvent prévenir une maladie grave après qu’une personne a été infectée. Au cours de la dernière année, des progrès significatifs ont été réalisés dans le développement de thérapies efficaces à base d’anticorps, et trois médicaments sont actuellement disponibles via une autorisation d’utilisation d’urgence (EUA) de la Food and Drug Administration.
Sotrovimab, la thérapie par anticorps la plus récente, a été développée par GlaxoSmithKline et Vir Biotechnology après qu’une grande étude collaborative menée par des scientifiques de tout le pays a découvert un anticorps naturel (dans le sang d’un survivant du SRAS, en 2003) qui a une ampleur et une efficacité remarquables.
Des expériences ont montré que cet anticorps, appelé S309, neutralise toutes les souches connues du SRAS-CoV-2 – y compris les mutants nouvellement apparus qui peuvent désormais « échapper » aux thérapies par anticorps précédentes – ainsi que le virus SARS-CoV original étroitement lié.
Jay Nix, chef du Consortium de biologie moléculaire basé à la source de lumière avancée (ALS) de Berkeley Lab, a utilisé des lignes de lumière à l’ALS et des lignes de lumière à la source lumineuse de rayonnement synchrotron de Stanford du SLAC pour effectuer une cristallographie aux rayons X sur des échantillons d’anticorps dérivés de survivants au cours d’une phase précoce de l’étude. Son travail, ainsi que d’autres résultats de cristallographie et de cryomicroscopie électronique, ont aidé à générer des cartes structurelles détaillées de la façon dont ces anticorps se lient à la protéine de pointe du SRAS-CoV-2, permettant à l’équipe au sens large de sélectionner les candidats les plus prometteurs et de les faire progresser vers la culture cellulaire. et des études animales. À la suite de résultats de laboratoire passionnants, les développeurs ont conçu le sotrovimab sur la base de la structure du S309 et l’ont évalué dans le cadre d’essais cliniques.
La FDA a accordé une EUA pour le sotrovimab fin mai après que des essais ont montré que les personnes atteintes d’infections légères à modérées au COVID-19 qui ont reçu une perfusion de la thérapie avaient une réduction de 85 % des taux d’hospitalisation ou de décès, par rapport au placebo.
Mais l’équipe ne s’est pas arrêtée là.
Comprenant que de nouvelles mutations pourraient survenir et qu’un nouveau coronavirus pathogène pourrait émerger d’un événement de croisement animal-humain, les scientifiques ont commencé une étude de suivi pour explorer en profondeur quels facteurs rendent les anticorps résistants à l’évasion virale et comment certains anticorps sont également largement réactifs contre divers virus apparentés. À l’aide d’analyses biochimiques et structurelles, d’un balayage mutationnel en profondeur et d’expériences de liaison, ils ont identifié un anticorps doté d’une puissance universelle sans précédent.
“Cet anticorps, qui se lie à un site auparavant inconnu sur la protéine de pointe du coronavirus, semble neutraliser tous les sarbecovirus connus – le genre de coronavirus qui provoque des infections respiratoires chez les mammifères”, a déclaré Nix, qui est affilié au Berkeley Lab’s Biosciences Area. “Et, en raison du site de liaison unique sur la partie résistante aux mutations du virus, il pourrait bien être plus difficile pour une nouvelle souche de s’échapper.”
Des tests ultérieurs sur des hamsters suggèrent que cet anticorps pourrait même prévenir une infection au COVID-19 s’il est administré à titre prophylactique. Le nouvel ouvrage a été publié dans La nature.
Référence : « Anticorps SARS-CoV-2 RBD qui maximisent la largeur et la résistance à l’évasion » par Tyler N. Starr, Nadine Czudnochowski, Zhuoming Liu, Fabrizia Zatta, Young-Jun Park, Amin Addetia, Dora Pinto, Martina Beltramello, Patrick Hernandez, Allison J. Greaney, Roberta Marzi, William G. Glass, Ivy Zhang, Adam S. Dingens, John E. Bowen, M. Alejandra Tortorici, Alexandra C. Walls, Jason A. Wojcechowskyj, Anna De Marco, Laura E. Rosen, Jiayi Zhou, Martin Montiel-Ruiz, Hannah Kaiser, Josh Dillen, Heather Tucker, Jessica Bassi, Chiara Silacci-Fregni, Michael P. Housley, Julia di Iulio, Gloria Lombardo, Maria Agostini, Nicole Sprugasci, Katja Culap, Stefano Jaconi, Marcel Meury, Exequiel Dellota, Rana Abdelnabi, Shi-Yan Caroline Foo, Elisabetta Cameroni, Spencer Stumpf, Tristan I. Croll, Jay C. Nix, Colin Havenar-Daughton, Luca Piccoli, Fabio Benigni, Johan Neyts, Amalio Telenti, Florian A. Lempp, Matteo S. Pizzuto, John D. Chodera, Christy M. Hebner, Herbert W. Virgin, Sean PJ Whelan, David Ve esler, Davide Corti, Jesse D. Bloom et Gyorgy Snell, 14 juillet 2021, La nature.
DOI : 10.1038 / s41586-021-03807-6
La source lumineuse avancée et la source lumineuse à rayonnement synchrotron de Stanford du SLAC sont des installations destinées aux utilisateurs du ministère de l’Énergie.
[ad_2]
Source link